临床试验常用缩写记不清?这有一份速查手册请(2)
【作者】网站采编
【关键词】
【摘要】简易新药申请程序,图源:作者 试验相关 IB(Investigator's Brochure)研究者手册,是有关试验用药品在进行人体研究时已有的临床与非临床资料。手册的作用
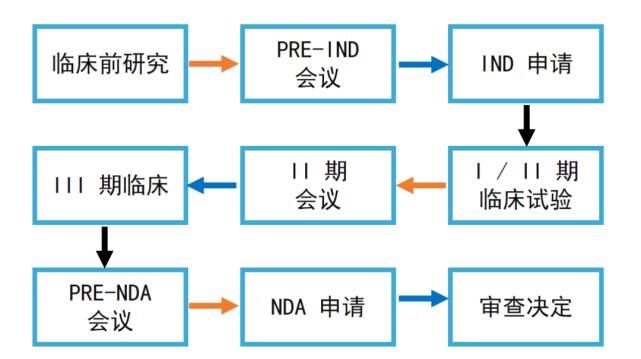 简易新药申请程序,图源:作者
简易新药申请程序,图源:作者
试验相关
IB(Investigator's Brochure)研究者手册,是有关试验用药品在进行人体研究时已有的临床与非临床资料。手册的作用主要为:给研究负责人提供所有有关被试药物的信息及研究结果;作为受试药物已获得正式核准的标志;包括所有最新的对受试药物所作研究的总结,这可用于新药临床试验或药物上市许可证的申请。
CRF表(Case Report Form)病例报告表,是在临床试验中用以记录每一名受试者在试验过程中的症状、体征或实验室检查数据的文件。
ICF(Informed Consent Form)知情同意书,是患者表示自愿进行医疗治疗的文件证明。根据「赫尔辛基宣言」、国际医学科学组织委员会(CIOMS)的「人体生物医学研究国际伦理指南」,国家食品药品监督管理局(CFDA)「药物临床试验质量管理规范」以及临床试验方案进行设计。采用受试者能够理解的文字和语言,使受试者能够「充分理解」,「自主选择」。知情同意书不应包含要求或暗示受试者放弃他们获得赔偿权利的文字,或必须举证研究者的疏忽或技术缺陷才能索取免费医疗或赔偿的说明。
EDC 系统( Electronic Data Capture System)电子数据捕获系统,是适用于临床试验数据采集和传输的平台软件。临床试验数据的采集是药物临床研究中的核心内容,真实、准确、及时、规范的数据采集能够显著提高临床试验的质量,缩短研究周期。EDC 系统采用电子化病例报告表(Electronic Case Report Form)?代替纸质病例报告表来对临床试验数据进行收集和管理。
策划:GoEun
题图:站酷海洛 Plus
文章来源:《基础医学与临床》 网址: http://www.jcyxylczz.cn/zonghexinwen/2021/0409/400.html